152) El impacto del blending hidrógeno en el gas natural
En el análisis anterior hemos observado el impacto de 20% hidrógeno en una red de gas natural. Sin embargo, como escuche en una reunión una vez, “La economía verde no saldrá con números rojos”. Actualmente, el precio del hidrógeno renovable puede rondar los 5-7 €/kg, y sabiendo que 1 kg de hidrógeno contiene un total de 33,3 kWh de energía, estamos hablando de 165-230 €/MWh.
Hoy en día, el precio del gas natural europeo ronda los 40 €/MWh, por lo que, el hidrógeno solo sería competitivo como combustible en escenarios donde el precio del gas natural fuera desorbitado, como, por ejemplo, el pico tras la Guerra de Ucrania en 2022 (+300 €/MWh). Cierto es que la sustitución de gas natural por hidrógeno traería consigo el concepto de emisiones de CO₂ abatidas, por el cual, nos ahorraríamos el impuesto al CO₂ (70 €/t CO₂). Asumiendo que la generación de un MWh emite unos 200 kg CO₂, estamos hablando de una penalización por las emisiones de unos 14 €/MWh. Por lo que, en la coyuntura actual no parece razonable quemar hidrógeno renovable desde el punto de vista económico.

Evidentemente, en un mundo descarbonizado la gran infraestructura gasista que España dispone está condenada a la irrelevancia si los combustibles fósiles se descartan. En ese escenario, se baraja la adicción del hidrógeno al gas natural para aprovechar las tuberías que están en operación. La combustión del hidrógeno (H₂), al no disponer de carbono en su estructura, no emite dióxido de carbono (CO₂). Así pues, son muchos los que abogan por el blending de hidrógeno para descarbonizar las redes de distribución, y sus posteriores usos aguas abajo. ¿Pero, de verdad, tiene sentido?
Impacto en el poder calorífico
La mezcla de gases que genera el bleding de hidrógeno NO aporta el mismo calor que la corriente inicial de 100% CH₄. No debemos olvidar, que la finalidad de una combustión siempre es la misma, obtener un calor, ya sea para un proceso industrial o para la calefacción; pero sobre todo, un calor constante.
Para comprender esto, lo mejor es analizar las diferencias entre los dos gases en sus estados puros, como podéis observar en la siguiente tabla, debido a su naturaleza, tienen diferentes características.
En la siguiente gráfica podéis ver como cambia el peso molecular de la mezcla H₂-CH₄, y análogamente, la evolución del poder calorífico másico de la mezcla.

El peso molecular de la mezcla desciende de manera constante, a medida que gradualmente incluimos el hidrógeno a la mezcla, aritmética pura. En cambio, el poder calorífico másico se ve muy influenciado por la densidad energética másica del hidrógeno. No nos olvidemos, que el hidrógeno pesa muy poco y ocupa mucho volumen a condiciones atmosféricas.
Por poner un ejemplo numérico he establecido una caldera de 277 kW que nos aporte un calor (1000 MJ/h) como objetivo de la mezcla, para de ese modo, normalizar los datos teniendo en cuenta la variación de cada una de los componentes. De este modo, con la corriente inicial de 100% CH₄, necesitaremos un caudal másico de 17,994 kg/h para obtener el calor fijado de 1000 MJ/h en el quemador.
Cual es la primera particularidad que se cruza en nuestro camino, a medida que vamos incluyendo 1, 2, 3, 4, 5 … 99% de Hidrógeno, y reduciendo en igual proporción el contenido en CH₄, ( por ejemplo 99% CH₄ + 1% H₂, 98% CH₄ + 2% H₂ … ), que el peso molecular del hidrógeno es 8 veces menor que el metano. Por lo tanto, cuando miramos el caudal másico (es decir, el caudal en masa), el meter hidrógeno no tiene apenas impacto, como podréis observar en la siguiente gráfica.

Como podéis comprobar, de la corriente inicial de 100% CH₄ a la corriente final de 100% H₂, se necesita 2,55 veces MENOS masa para obtener el mismo calor en la combustión. Sin embargo, el hidrógeno no se encuentra en estado sólido, sino en gas. Por lo que sería, más adecuado hablar en volumen, que en masa. Ya que, en el caudal másico era relevante la densidad energética gravimétrica (MJ/kg), pero en el caudal molar, lo relevante es la densidad energética volumétrica (MJ/m³). De este modo, con la corriente inicial de 100% CH₄, necesitaremos un caudal másico de 1,122 kmol/h para obtener el calor fijado de 1000 MJ/h en la combustión.
Todos os acordareis que en el colegio en la asignatura de Química se daba la ley de los gases ideales, la cual se regia por PV = n RT. De esa formula podemos sacar, que 1 mol de gas, ocupa 22,4 L a condiciones estándares de presión y temperatura.
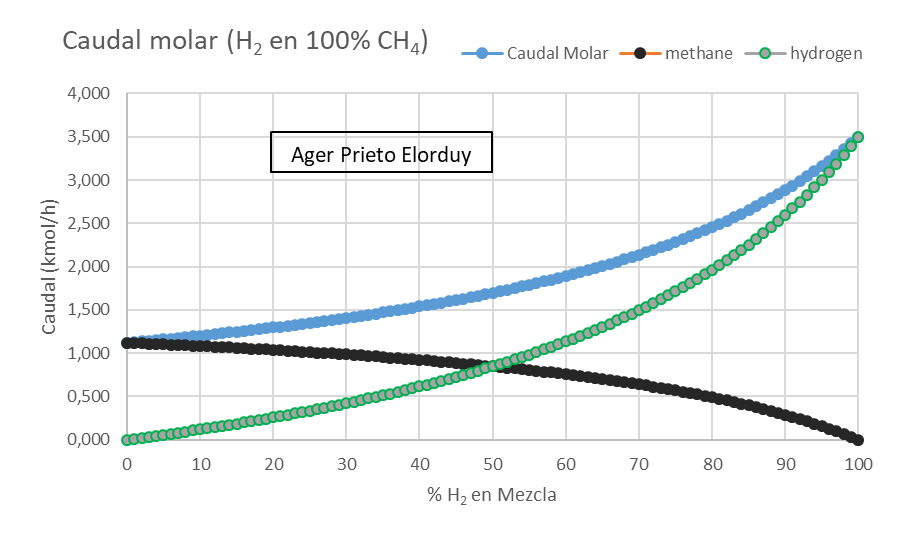
Como podéis comprobar, de la corriente inicial de 100% CH₄ a la corriente final de 100% H₂, se necesita 3,11 veces MÁS moles (= volumen) para obtener el mismo calor en la combustión.
Entonces, que observamos, que para lograr el mismo calor que lográbamos con 100% CH₄, la tendencia de la reducción de emisiones de CO₂ al hacer blending de Hidrógeno, NO ES LINEAL, tiene FORMA DE TIRO PARABÓLICO.

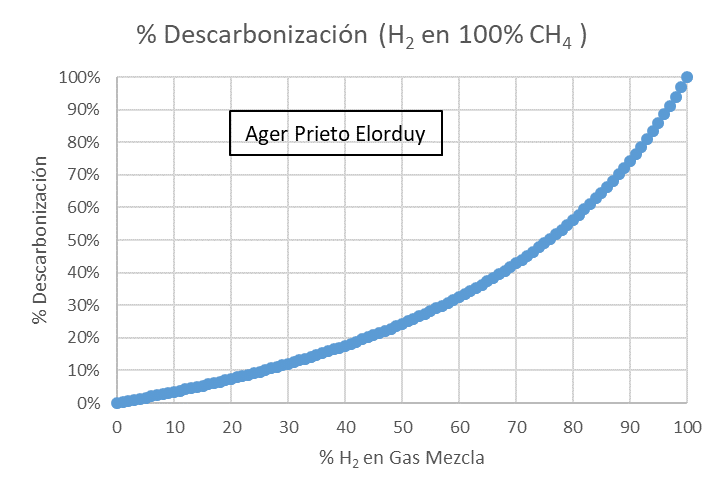
En la siguiente gráfica podemos comprobar lo poco que descarboniza hacer blending de hidrógeno en una corriente de 100% metano. Pensad que el gas natural es +90% metano, y el resto lo conformar otros hidrocarburos como etano, propano, butano… Por lo que, estamos ante el mismo escenario.
Como podéis observar en el gráfico: Un 25% de adicción de H₂, descarboniza un 10%, un 50% de adicción de H₂, descarboniza un 24% y un 75% de adicción de H₂, descarboniza un 48%.
Por lo que, si queremos convertir en más sostenible el gas natural (combustible fósil) el blending de hidrógeno tiene un impacto limitado. Ya que como se ha demostrado durante este análisis, la reducción de emisiones que se logra es mínima. Otra cosa distinta es, que sea una corriente 100% hidrógeno, eso si descarboniza.
He realizado el mismo ejercicio para el resto de hidrocarburos gaseosos (corrientes 100 %), y seguidamente podéis observar la descarbonización que se genera.

Es evidente que cuanto mayor es el peso molecular del hidrocarburo gaseoso, menor es la descarbonización que se logra con el blending de hidrógeno, y por lo tanto, menor es la reducción de las emisiones de CO₂ asociado a ello.
Intercambio de familia de gases - Índice de Wobbe
Pero cuando se va a realizar la combustión de una mezcla de gases, al tratarse de dos gases con diferentes características es necesario saber si pueden mezclarse para dar una combustión adecuada. Para ello, Goffredo Wobbe observó en 1927 que los gases con valores similares del Índice de Wobbe podían intercambiarse en procesos de calentamiento.
Al final al cabo se emplea para comparar la producción de energía de combustión de diferentes gases combustibles sin conocer su composición detallada (algo habitual en el gas natural, dado que las concentraciones de los gases que conforman el gas natural (metano/etano/ propano/butano …), no son constantes a lo largo del tiempo, ni iguales según el origen del yacimiento.

Es por eso, que cada país marca por normativa el rango admisible para cada gas. Es decir, que indica los máximos o mínimos que deberían existir dentro de una mezcla.
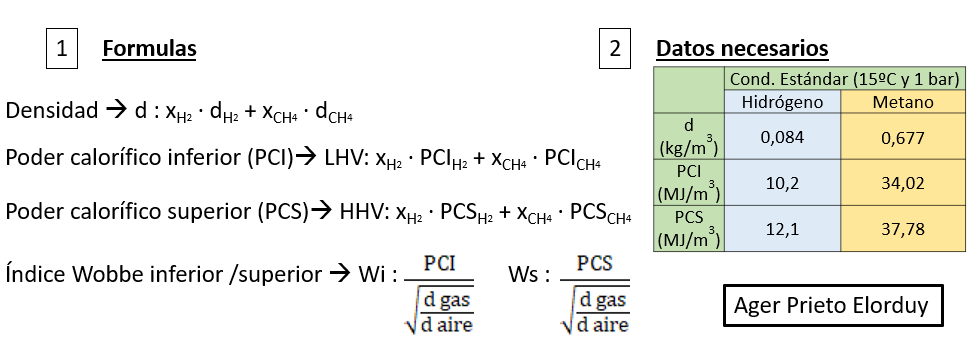
Índice de Wobbe se define como la relación del poder calorífico superior (High Heating Value, HHV) por unidad de medida del gas a la raíz cuadrada de la densidad relativa del gas (definido como densidad del gas/densidad del aire seco). En la imagen adjunta podréis observar las formulas necesarias para calcular el índice de Wobbe.
Destacar que la densidad de una mezcla de gases se puede calcular, sabiendo los porcentajes del gas respecto a la mezcla y la densidad de cada gas.
El poder calorífico inferior, en ingles Low Heating Value (LHV), hace referencia a la cantidad total de calor desprendido en la combustión completa de 1 kg de combustible sin contar la parte correspondiente al calor latente del vapor de agua de la combustión, ya que no se produce cambio de fase, y se expulsa como vapor.
El Índice de Wobbe es un factor crítico para minimizar el impacto de fluctuaciones en el suministro de gas combustible y aumentar la eficiencia del sistema de combustión porque los equipos diseñados para operar en un cierto Índice de Wobbe generalmente tienen una tolerancia de solo ~5% . Si dos combustibles tienen índices de Wobbe idénticos para la misma presión y los ajustes de válvula dados, la energía la salida también será idéntica.
En la siguiente tabla podéis comprobar porque es importante saber calcular el índice de Wobbe, ya que, es el parámetro que se emplea para agrupar los gases en tres familias. Es decir, las familias de dividen en grupos en función del poder calorífico que aporta la hacer combustión de dicha mezcla gaseosa.
Primera familia
La primera familia hace referencia al gas ciudad (mezcla de hidrocarburos con gran contenido en hidrógeno), gas que se utilizaba en el siglo XIX hasta la mitad del siglo XX para iluminar calles y viviendas y, también, para calentar y cocinar en las casas. Al principio se obtenía en fábricas destilando hulla (carbón mineral de color negro mate procedente de sedimentos enterrados de grandes masas vegetales). Más adelante, dejaron de usar carbón y empezaron a usar las naftas, un producto derivado de la destilación del petróleo, con una composición basada en hidrógeno e hidrocarburos. Su combustión era muy luminosa y, popularmente, el gas ciudad se empezó a conocer como “luz de alumbrado”. Su alto contenido de monóxido de carbono lo convertía en un producto muy peligroso para la salud, al inhalar el monóxido de carbono, pasa a la sangre a través de los pulmones y evita que la hemoglobina trasporte el oxígeno, generando el ahogamiento por desplazamiento.
Segunda familia
Entre que era complejo fabricar gas cuidad y los problemas de seguridad que ocasionaba, el mundo transicionó hacia otra familia de gases, la segunda familia, donde se enmarca el gas natural que nos llega a prácticamente todos nosotros. De la Imagen 11 podemos observar que el rango del índice de Wobbe es de 39,1-54,7 MJ/m³ , por lo ya sabemos que se consigue más calor que con la primera familia. Cabe destacar que esta familia de gases contiene tres subgrupos (L, E y H). En el caso de España, el gas natural se engloba en la Familia 2H, y contiene un índice de Wobbe de 45,7-54,7 MJ/m³.
Tercera familia
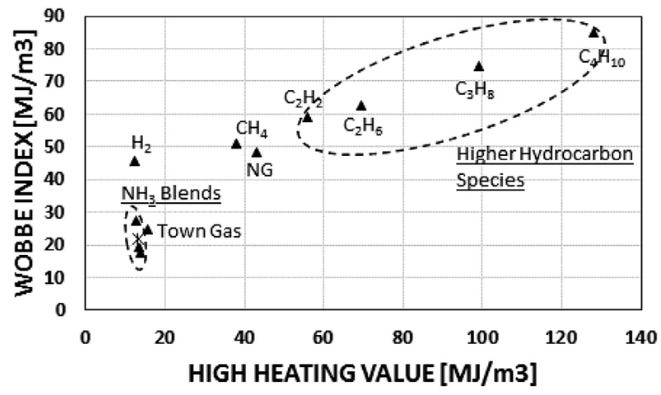
Está última familia engloba al Gas Licuado de Petróleo (GLP). El GLP es un gas que contiene una mezcla de propano y butano. Es por eso, que si la mezcla es mayoritariamente propano, el gas se cataloga como subgrupo P. En cambio, si la fracción principal es el butano, el subgrupo es B. Del Índice de Wobbe observamos que el GLP nos entrega más calor en la combustión. En la siguiente gráfica podéis observar como evoluciona el poder calorífico superior (HHV, en el eje X) y el índice de Wobbe (en el eje Y). Queda claro, que a mayor peso molecular del hidrocarburo gaseoso, mayor será el poder calorífico contenido en su interior.
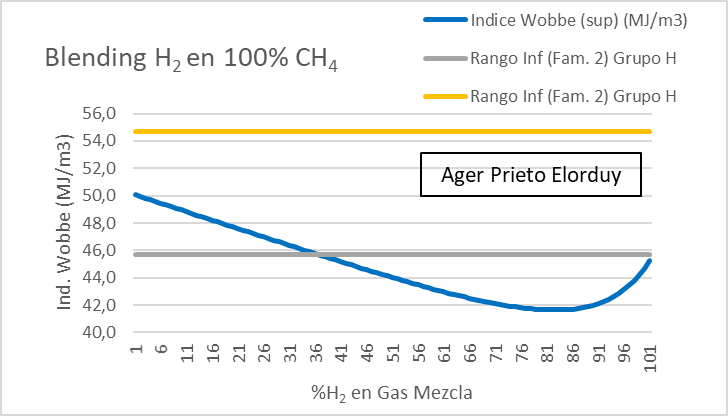
Pero volviendo al caso que nos ataña, he estudiado el blending creciente de hidrógeno en una corriente de 100% metano (CH₄). Fijaros que el índice de Wobbe describe una trayectoria, que parece el símbolo de Nike invertido. Ya que, el 100 % de hidrógeno tiene un índice de Wobbe idéntico al de la mezcla de 40 % de hidrógeno y 60 % de metano.
Destacar que a partir de un 35%, la nueva mezcla de gases generada, deja de pertenecer a la familia de gases 2H, y en ese caso, el quemador industrial estaría operando fuera de rango.
Riesgo de la llama
En la siguiente imagen, se puede ver como el blending de hidrógeno sobre el gas natural aumenta la temperatura de la llama adiabática que se genera. Aproximadamente, unos 200 K más respecto a la llama de 100% gas natural.

La temperatura de la llama de hidrógeno se puede reducir, por ejemplo:
-Aumentando el exceso de aire de combustión (como se observa en la gráfica anterior cuando el ratio estequiométrico supera 1).
-Utilizando la recirculación de gases de combustión.
Otra estrategia es reducir el tiempo de residencia:
-Aumentando la velocidad de la mezcla de hidrógeno/aire.
-Mejorando la mezcla de los reactivos.
-Reduciendo simultáneamente el tiempo de residencia de estos reactivos en los puntos calientes de la llama.
La velocidad laminar se define como la velocidad a la que se propaga un frente de llama con respecto al gas no quemado para una llama premezclada que se propaga libremente en una dimensión.
La LLAMA ES ESTABLE, cuando la velocidad del flujo y la velocidad de propagación del frente de la llama son IGUALES.
LLAMA SE DESPRENDE, cuando la velocidad de propagación del frente de llama es MAYOR que la velocidad del flujo.
LLAMA RETROCEDE, cuando la velocidad de propagación del frente de llama es MENOR que la velocidad del flujo.

El desprendimiento tampoco es correcto, sin embargo, el retroceso de la llama es MUY PELIGROSO para la seguridad. Para ello, se emplea el potencial de combustión, C, es una medida indirecta (proporcional) de la velocidad de propagación de la llama producida en la combustión del gas, representando por tanto su tendencia al soplado o calado. El potencial de combustión de una mezcla se calcula relacionando % volumétrico de cada componente presente en el gas con una constante intrínseca de cada gas puro y la densidad relativa del gas con respecto al aire.
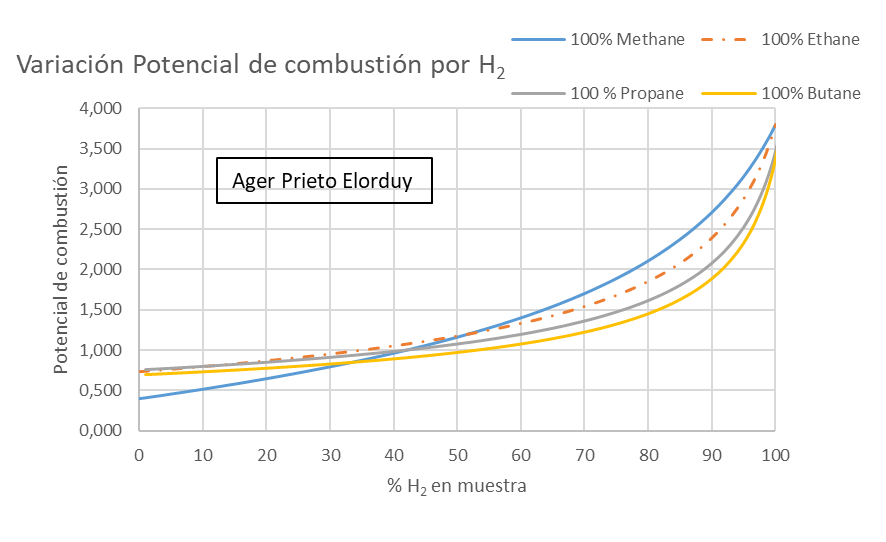
-Cuanto mayor es el valor de C, mas corta es la llama. Por lo que aumenta la posibilidad de que se produzca retroceso de llama.
-Cuanto menor es el valor de C, más larga es la llama, aumentando la probabilidad de que se produzca un desprendimiento de llama.
Por lo que, el blending de hidrógeno en el gas natural aumenta la posibilidad de retroceso de la llama.
Después de este extenso análisis las conclusiones parecen claras. La mezcla de hidrógeno/gas natural tiene menor poder calorífico, es decir, para lograr el mismo rendimiento energético el caudal tiene que aumentar. A partir de un 35% hidrógeno, la nueva mezcla de gases generada, deja de pertenecer a la familia de gases 2H, y en ese caso, el quemador industrial estaría operando fuera de rango. A su vez, la adicción del hidrógeno incrementa el riesgo del retroceso de llama, lo que deriva en un claro riesgo de seguridad debido a la posibilidad de explosión.
La combustión de una mezcla de hidrógeno/gas natural tiene sus peculiaridades, que por su relevancia, han de tenerse en cuenta. Si a ese escenario, le añadimos un precio elevado del hidrógeno renovable como hemos visto al inicio, no parece que vaya ser un uso relevante en la industria. Al menos, hasta que el desarrollo del sector de hidrógeno sea tal, donde los electrolizadores sean un equipo industrial común, y existan excedentes que no se sepa valorizar de otra manera.